
pH ของสารละลาย
ในสารละลายกรดหรือเบสจะมีทั้ง H3O+ และ OH– อยู่ในปริมาณที่แตกต่างกัน การบอกความเป็นกรด เป็นเบสของสารละลายโดยใช้ความ
เข้มข้นของ H3O+ หรือ OH– มักเกิดความผิดพลาดได้ง่ายเพราะสารละลายมักมีความเข้มข้นของ H3O+ หรือ OH– น้อย ดังนั้นในปี ค.ศ. 1909 นักเคมีชาวสวีเดนชื่อ ซอเรสซัน (Sorensen) ได้เสนอให้บอกความเป็นกรด-เบสของสารละลายในรูปมาตราส่วนpH ย่อมาจากภาษาฝรั่งเศสว่า puissance d,hydrogine แปลว่า กำลังของไฮโดรเจน (power of hydrogen) โดยกำหนดว่า

เมื่อความเข้มข้นของ H3O+ มีหน่วยเป็น mol/dm3 หรือ Molar
ในสารละลายที่เป็นกลาง [H3O+] = [OH–] = 1.0 x 10-7 mol/dm3
ดังนั้น หา pH ของสารละลายได้ดังนี้ pH = – log[H3O+]
= – log 1.0 x 10-7
= – (log 1.0 – 7log10)
= 0 + 7 = 7
นั่นคือสารละลายที่เป็นกลางมี pH = 7
ค่า pH ที่ใช้ระบุความเป็นกรดหรือเบสของสารละลาย สรุปได้ดังนี้
สารละลายกรด มี [H3O+] มากกว่า 1.0 x 10-7 mol/dm3 ดังนั้น pH<7.00
สารละลายที่เป็นกลาง มี [H3O+] เท่ากับ 1.0 x 10-7 mol/dm3 ดังนั้น pH = 7.00
สารละลายเบส มี [H3O+] น้อยกว่า 1.0 x 10-7 mol/dm3 ดังนั้น pH>7.00

นอกจากนี้สามารถบอกความเป็นกรด-เบสของสารละลายในรูปความเข้มข้นของ OH– ก็ได้ โดยค่า pOHค่า pOH ใช้บอกความความเป็นกรด-
เบสของสารละลายเจือจางได้เช่นเดียวกับค่า pH ซึ่งค่า pOH จะขึ้นอยู่กับความเข้มข้นของ OH– โดยกำหนดความสัมพันธ์ดังนี้

ตัวอย่างการคำนวณค่า pOH
สารละลาย NaOH เข้มข้น 0.01 โมลต่อลูกบาศก์เซนติเมตร มี pH เท่าใด
วิธีทำ NaOH (aq) ————-> Na+ (aq) + OH– (aq)
0.01 mol/dm3 0.01 mol/dm3 = 1 x 10-2 mol/dm3
pOH = -log[OH–]
= -log 1×10-2 mol/dm3
= 2log10 – log1
pOH = 2

ในสารละลายที่เป็นกลางซึ่งมี [OH–] = 1.0 x 10-7 mol/dm3 จะมี pOH = 7
ความสัมพันธ์ระหว่าง pH กับ pOH
[H3O+][ OH–] = 1.0 x 10-14
log[H3O+][ OH–] = log1.0 x 10-14
log[H3O+] + log[OH–] = log1.0 – 14 log10
– log[H3O+] – log[OH–] = 14 log10

มาตราส่วน pH (pH scale) ใช้บอกความเป็นกรด-เบสของสารละลาย
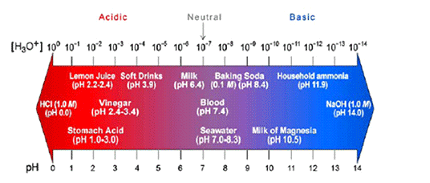
(ที่มา : สุนทร พรจำเริญ เอกสารประกอบการสอนเรื่องกรด-เบส โรงเรียนมหิดลวิทยานุสรณ์)
ตารางแสดง สเกล pH ของสารละลายที่มีความเข้มข้นต่างๆ กัน
 |
วิธีวัด pH ของสารละลายวัดได้ 2 วิธี ดังนี้
1. วิธีเปรียบเทียบสี วิธีนี้เป็นการวัด pH โดยประมาณ (มีความถูกต้อง 0.5 หน่วย pH) ซึ่งทำได้โดยเติมอินดิเคเตอร์ที่เหมาะสมลงไปในสารละลายที่ต้องการวัด pH แล้วเปรียบเทียบกับสารละลาย ทำได้โดยเติมอินดิเคเตอร์ที่เหมาะสมลงไปในสารละลายที่ต้องการวัด pH แล้วเปรียบเทียบสีกับสารละลายบัฟเฟอร์ที่ทราบค่า pH แน่นอน ซึ่งได้เติมอินดิเคเตอร์ชนิดเดียวกันไปแล้ว หรือใช้กระดาษชุบอินดิเคเตอร์ (กระดาษ pH) จุ่มลงไปแล้วเปรียบเทียบกับสีมาตรฐาน
2. วิธีวัดความต่างศักย์ วิธีนี้วัด pH ได้อย่างละเอียด (มีความถูกต้อง 0.01 หน่วย pH) โดยการใช้เครื่องมือที่เรียกว่า พีเอชมิเตอร์ ซึ่งวัด pH ของสารละลายได้โดยการวัดความต่างศักย์ระหว่างขั้วไฟฟ้า 2 ขั้ว

ภาพแสดงเครื่องพีเอชมิเตอร์
http://www.ponpe.com/component/option,com_virtuemart/page,shop.browse/category_id,30/Itemid,90/vmcchk,1/

