
อิเล็กโทรไลต์ (Electrolyte) หมายถึง สารที่เมื่อละลายในน้ำจะนำไฟฟ้าได้ เนื่องจากมีไอออนซึ่งอาจจะเป็นไอออนบวก หรือไอออนลบเคลื่อนที่อยู่ในสารละลาย สารละลายอิเล็กโทรไลต์นี้อาจเป็นสารละลายกรด เบส หรือเกลือก็ได้ ตัวอย่างเช่น สารละลายกรดเกลือ (HCl) สารละลายโซเดียมไฮดรอกไซด์ (NaOH) และสารละลายของเกลือ KNO3 เป็นต้น โดยในสารละลายดังกล่าวประกอบด้วยไอออน H+ , Cl– , OH– , K+ และ NO3 – ตามลำดับ
นอนอิเล็กโทรไลต์ (Non-electrolyte) หมายถึง สารที่ไม่สามารถนำไฟฟ้าได้เมื่อละลายน้ำ ทั้งนี้เนื่องจาก สารพวกนอนอิเล็กโทรไลต์ จะไม่สามารถแตกตัวเป็นไอออนได้ เช่น น้ำบริสุทธิ์ น้ำตาล แอลกอฮอล์ เป็นต้น ความแตกต่างของสารอิเล็กโทรไลต์และนอน- อิเล็กโทรไลต์ พิจารณาจากสาร 2 ชนิด เมื่อละลายน้ำจะรวมกับน้ำเกิดการเปลี่ยนแปลงดังนี้

ภาพการเป็นอิเล็กโทรไลต์และนอนอิเล็กโทรไลต์ของสาร
อิเล็กโทรไลต์แก่และอิเล็กโทรไลต์อ่อน
สารละลายอิเล็กโทรไลต์ต่างๆ นำไฟฟ้าได้ไม่เท่ากัน เนื่องจากการแตกตัวเป็นไอออนของอิเล็กโทรไลต์ไม่เท่ากัน อิเล็กโทรไลต์ที่แตกตัวเป็นไอออนได้มากกว่า ก็จะนำไฟฟ้าได้ดีกว่าอิเล็กโทรไลต์ที่แตกตัวเป็นไอออนได้น้อยกว่า อิเล็กโทรไลต์แบ่งออกได้เป็น 2 ประเภท ดังนี้
1. อิเล็กโทรไลต์แก่ (strong electrolyte) หมายถึง สารที่ละลายน้ำแล้วแตกตัวเป็นไอออนได้มาก อาจจะแตกตัวได้ 100% และนำไฟฟ้าได้ดีมาก เช่น กรดแก่ และเบสแก่ และเกลือส่วนใหญ่จะแตกตัวได้ 100% เป็นต้น
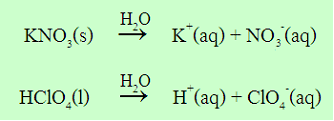
ตัวอย่างสมการแสดงการแตกตัวของสารละลายอิเล็กโทรไลต์แก่
2. อิเล็กโทรไลต์อ่อน (weak electrolyte) หมายถึง สารที่ละลายน้ำแล้วแตกตัวได้บางส่วน นำไฟฟ้าได้น้อย
ตัวอย่างสมการแสดงการแตกตัวของสารละลายอิเล็กโทรไลต์อ่อน

ตารางตัวอย่างของอิเล็กโทรไลต์แก่ และอิเล็กโทรไลต์อ่อนบางชนิด
อิเล็กโทรไลต์แก่(นำไฟฟ้าได้ดี) |
อิเล็กโทรไลต์อ่อน(นำไฟฟ้าได้ไม่ดี) |
เกลือที่ละลายน้ำทั้งหมดH2SO4HNO3HCIHBrHCIO4NaOHKOHCa(OH)2Ba(OH)2 |
CH3COOHH2CO3HNO2H2SO3H2SH2C2O4H3BO3HCIONH4OHHF |
เราจะรู้ได้อย่างไรว่าสารละลายของเราเป็นสารละลายอิเล็กโทรไลต์หรือเปล่า?
ตัวอย่างผลการทดลองการทดสอบการนำไฟฟ้า
สารที่ใช้ทดสอบ |
ผลการทดสอบ |
น้ำบริสุทธิ์น้ำที่มีน้ำตาลละลายอยู่ยูเรีย CO(NH2)2สารละลายเกลือ NaClสารละลายเกลือ K2SO4สารละลายกรด HCIสารละลายกรดแอซิติก CH3COOHสารละลายเบส NaOHสารละลายเบส Na4OH |
ไม่นำไฟฟ้า (หลอดไฟไม่สว่าง)ไม่นำไฟฟ้า (หลอดไฟไม่สว่าง)ไม่นำไฟฟ้า (หลอดไฟไม่สว่าง)นำไฟฟ้า (หลอดไฟสว่าง)นำไฟฟ้า (หลอดไฟสว่าง)นำไฟฟ้า (หลอดไฟสว่าง)นำไฟฟ้าน้อย (หลอดไฟสว่าง)นำไฟฟ้า (หลอดไฟสว่าง)นำไฟฟ้า (หลอดไฟสว่าง) |
ผลที่ได้อธิบายได้ว่า สารละลายที่ไม่มีไอออนอยู่ เช่น น้ำ หรือน้ำตาลทรายที่ละลายอยู่ในน้ำมัน จะมีพันธะแบบโคเวเลนต์ ไม่สามารถแตกตัวเป็นไอออนได้ จึงไม่นำไฟฟ้า แต่ NaCl HCl เมื่ออยู่ในน้ำจะแตกตัวเป็น Na+ , Cl– หรือ H+ , Cl– ซึ่งเป็นไอออนที่เคลื่อนที่ในสารละลายทำให้เกิดการนำไฟฟ้าขึ้นได้
