การแตกตัวของกรดแก่
กรดแก่ หมายถึงกรดที่เมื่อละลายน้ำแล้วสามารถแตกตัวเป็นไอออนได้ 100 %
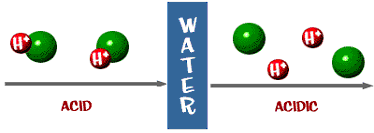
ให้สังเกตการแตกตัวของกรดแก่ HCl เปรียบเทียบกับการแตกตัวของกรดอ่อน HF ซึ่งการแตกตัวเป็นดังสมการ
HCl(aq) ——-> H +(aq) + Cl–(aq)
0.1 mol/dm3 0.1 mol/dm3 0.1 mol/dm3
HF(aq) 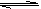 H +(aq) + F–(aq)
H +(aq) + F–(aq)
0.1 mol/dm3 x mol/dm3 x mol/dm3
ตัวอย่างกรดแก่สามัญ ได้แก่
|
สูตรเคมี |
ชื่อกรด |
|
HCl |
ไฮโดรคลอริก(hydrochloric acid) |
|
HBr |
ไฮโดรโบรมิก(hydrobromic acid) |
|
HI |
ไฮโดรไอโอดิก(hydroiodic acid) |
|
HNO3 |
ไนตริก(nitric acid) |
|
HClO4 |
เปอร์คลอริก(perchloric acid) |
|
H2SO4 |
ซัลฟิวริก(sulfuric acid) |
กรด HCl HBr HI HNO3 HClO4 เป็นกรดที่ 1 โมเลกุลสามารถแตกตัวให้ 1 H+ เรียกกรดที่ 1 โมเลกุลแตกตัวให้ 1 H+ นี้ว่ากรดมอนอโปรติก(monoprotic) ซึ่งการแตกตัวของกรดแก่มอนอโปรติก จะมีลักษณะคล้ายกันคือแตกตัวให้ H+(ซึ่งรวมกับน้ำกลายเป็นไฮโดรเนียมไอออน(H3O+)) และไอออนลบที่มีความเข้มข้นเท่ากันและเท่ากับความเข้มข้นของกรด ดังสมการ
HA(aq) + H2O(l) —–> A–(aq) + H3O+(aq)
ตัวอย่าง HClO4(aq) + H2O(l) —–> ClO4–(aq) + H3O+(aq)
2 mol 2 mol 2 mol
0.5 mol/dm3 0.5 mol/dm3 0.5 mol/dm3
HNO3(aq) + H2O(l) —–> NO3–(aq) + H3O+(aq)
3 mol 3 mol 3 mol
0.6 mol/dm3 0.6 mol/dm3 0.6 mol/dm3
สรุป กรดแก่มอนอโปรติกความเข้มข้นของไฮโดรเนียม = ความเข้มข้นของกรดหรือ [H3O+] = [HA] |
กรณีกรดแก่ H2SO4 เป็นกรดที่ 1 โมเลกุลสามารถแตกตัวให้ H+ ได้ 2 ไอออนซึ่งเรียกว่ากรด diprotic ซึ่งกรดที่สามารถแตกตัวให้ H+ หลายไอออนอาจเรียกรวมๆ ว่ากรด polyprotic กรด H2SO4 สามารถแตกตัวได้ 2 ขั้น ดังนี้
ขั้นที่ 1 H2SO4 เป็นกรดแก่แตกตัวได้ 100%
H2SO4 + H2O —–> HSO4– + H3O+
2 mol 2 mol 2 mol
0.3 mol/dm3 0.3 mol/dm3 0.3 mol/dm3
ขั้นที่ 2 HSO4– เป็นกรดอ่อนจะแตกตัวบางส่วนเกิดภาวะสมดุล ความสัมพันธ์ระหว่างความเข้มข้นของสาร ณ ภาวะสมดุลเป็นดังนี้
HSO4– + H2O SO42- + H3O+
0.3-x mol/dm3 x mol/dm3 x mol/dm3
แต่ในระดับมัธยม มักกำหนดให้ H2SO4 แตกตัว 100% จึงเขียนสมการและความสัมพันธ์ระหว่างโมลหรือความเข้มข้นของสารดังนี้
H2SO4 + 2H2O —–> SO42- + 2H3O+
2 mol 2 mol 4 mol
0.3 mol/dm3 0.3 mol/dm3 0.6 mol/dm3
0.625×10-4 mol/dm3 0.625×10-4 mol/dm3 1.25×10-4 mol/dm3
ดังนั้น ความเข้มข้นของไฮโดรเนียม = 2 เท่าของความเข้มข้น H2SO4 หรือ [H3O+] = 2[H2SO4] |
การแตกตัวของเบสแก่
เบสแก่ หมายถึงเบสที่เมื่อละลายน้ำแล้วสามารถแตกตัวเป็นไอออนได้ 100 %
ตัวอย่างเบสแก่ ได้แก่
|
สูตรเคมี |
ชื่อเบส |
|
LiOH |
ลิเทียมไฮดรอกไซด์(lithium hydroxide) |
|
NaOH |
โซเดียมไฮดอรกไซด์ (sodium hydroxide) |
|
KOH |
โพแตสเซียมไฮดรอกไซด์(potassium hydroxide) |
|
RbOH |
รูบิเดียมไฮดรอกไซด์(rubidium hydroxide ) |
|
CsOH |
ซีเซียมไฮดรอกไซด์(caesium hydroxide) |
|
Ca(OH)2 |
แคลเซียมไฮดรอกไซด์(calcium hydroxide) |
|
Ba(OH)2 |
แบเรียมไฮดรอกไซด์(balium hydroxide) |
|
Sr(OH)2 |
สทรอนเชียมไฮดรอกไซด์(strontrium hydroxide) |
สารประกอบไฮดรอกไซด์ของธาตุหมู่ 1 ซึ่งมีสูตรทั่วไป XOH เมื่อละลายน้ำจะแตกตัวให้ไอออนบวกและไฮดรอกไซด์ไอออน โดยโมลหรือความเข้มข้นของไอออนบวก ไฮดรอกไซด์ไอออนและเบสจะเท่ากัน ดังสมการ
XOH(aq) ——> X+(aq) + OH–(aq)
ตัวอย่าง NaOH(aq) ——> Na+(aq) + OH–(aq)
KOH(aq) ——> K+(aq) + OH–(aq)
2 mol 2 mol 2 mol
0.5 mol/dm3 0.5 mol/dm3 0.5 mol/dm3
สรุป สำหรับเบสแก่ XOH
|
[OH–] = [XOH–] |
สารประกอบไฮดรอกไซด์ของธาตุหมู่ 2 ซึ่งมีสูตรทั่วไป Y(OH)2 เมื่อละลายน้ำจะแตกตัวให้ไอออนบวกและไฮดรอกไซด์ไอออน โดยโมลหรือความเข้มข้นของไฮดรอกไซด์ไอออนจะเป็นสองเท่าของโมลหรือความเข้มข้นของไอออนบวกและเบส ดังสมการ
Y(OH)2(aq) ——> Y2+(aq) + 2OH–(aq)
ตัวอย่าง Ca(OH)2(aq) ——> Ca2+(aq) + 2OH–(aq)
Ba(OH)2(aq) ——> Ba2+(aq) + 2OH–(aq)
2 mol 2 mol 4 mol
0.3 mol/dm3 0.3 mol/dm3 0.6 mol/dm3
0.25×10-4 mol/dm3 0.25×10-4 mol/dm3 0.50×10-4 mol/dm3
สรุป สำหรับเบส Y(OH)2
|
[OH–] = 2[Y(OH)2] |
ตัวอย่างการคำนวณเกี่ยวกับการแตกตัวของกรดแก่และเบสแก่
ตัวอย่างที่ 1 จงคำนวณหา [H3O+] , [NO3–] ในสารละลาย 0.015 M HNO3
วิธีทำ HNO3 +H2O → H3O+ + NO3–
0.015
เพราะฉะนั้น [H3O+] = [NO3–] = 0.015 โมล/ ลิตร
ตัวอย่างที่ 2 ถ้า KOH 0.1 โมล ละลายน้ำและสารละลายมีปริมาตร 2 ลิตร ในสารละลาย
จะมีไอออนใดบ้างอย่างละกี่โมลต่อลิตร
วิธีทำ KOH (s) → K+ (aq) + OH– (aq)
0.1โมล/ 2 ลิตร
สารละลาย KOH 2 ลิตร มี KOH 0.1 โมล
สารละลาย KOH 1 ลิตร มี KOH = 0.05 โมล/ ลิตร
ดังนั้น KOH จะแตกตัวให้ K+ และ OH– อย่างละ 0.05 โมล/ ลิตร
ตัวอย่างที่ 3 สารละลายกรดแก่ (HA) 250 ลูกบาศก์เซนติเมตร มีปริมาณ H3O+ ไอออน 0.05 โมล สารละลายนี้มีความเข้มข้นเท่าใด ถ้าเติมกรดนี้ลงไปอีก 0.2 โมล โดยที่สารละลายมีปริมาตรคงเดิม สารละลายที่ได้จะมีความเข้มข้นเท่าใด
วิธีทำ HA → H3O+ (aq) + A– (aq)
0.05 โมล/ 250 cm3
สารละลาย HA 250 cm3 มี HA 0.05 โมล
สารละลาย HA1000cm3มี HA = = 0.20โมล
เพราะฉะนั้นสารละลายที่ได้มีความเข้มข้น0.20โมล/ ลิตร
ถ้าเติมกรดอีก 0.2 โมล
สารละลายมี HA รวมทั้งหมด = 0.05 + 0.2 = 0.25 โมล
สารละลาย HA 250 cm3มี HA 0.25 โมล
สารละลายHA1000cm3มี HA = = 1.00 โมล
เพราะฉะนั้นสารละลายที่ได้มีความเข้มข้น1.00โมล/ ลิตร
ตัวอย่างที่ 4 จงหาความเข้มข้นของ OH– ที่เกิดจากการเอา NaOH 10.0 กรัม ละลายในน้ำทำเป็นสารละลาย 0.2 dm3 (Na = 23, O = 16, H = 1)
วิธีทำ จำนวนโมลของ NaOH = = 0.25 mol
สารละลาย 0.2 dm3 มีเนื้อของ NaOH = 0.25 โมล
สารละลาย 1 dm 3มี NaOH = = 1.25 โมล/ ลิตร
เพราะฉะนั้นสารละลายมีความเข้มข้น 1.25 โมล/ ลิตร
และปฏิกิริยาการแตกตัวของ NaOH เป็นดังนี้
NaOH (aq) → Na+ (aq) + OH– (aq)
1.25 โมล 1.25 โมล 1.25 โมล
เพราะฉะนั้นความเข้มข้นของ OH– = 1.25โมล/ ลิตร
